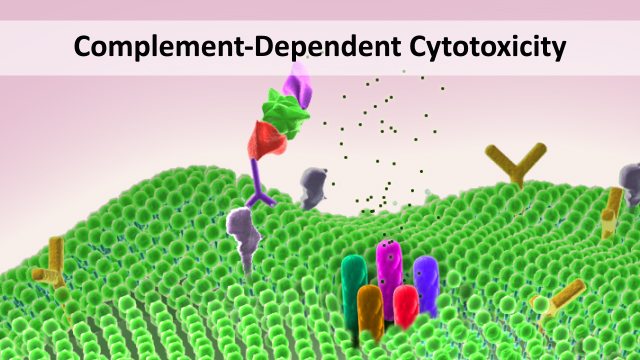
 Բջջային ցիտոտոքսիկությունը իմունային պատասխանի կարևոր մեխանիզմն է:
Բջջային ցիտոտոքսիկությունը իմունային պատասխանի կարևոր մեխանիզմն է:
Ցիտոտոքսիկությունը մեխանիզմ է, որի օգնությամբ լեյկոցիտները ի վիճակի են ճանաչել և քայքայել այլ բջիջներ: Բջջային ցիտոտոքսիկությունը պաշտպանում է հետևյալի դեմ'
- Ներբջջային պաթոգենների,այդ թվում և վիրուսների,
- Որոշ բակտերիաների,
- Որոշ պարազիտների:
Ցիտոտոքսիկ բջիջների թիրախ կարող են հանդիսանալ ուռուցքներ,պաթոգեն էուկարիոտներ և անգամ օրգանիզմի սեփական բջիջները: Այն կարևոր դեր է խաղում ալոգեն տրանսպլանտատների մերժման մեջ: Հայտնի են հետևյալ ցիտոտոքսիկ բջիջները'
- Ցիտոտոքսիկ T-լիմֆոցիտներ(CTL),
- Բնական քիլլերներ (NK),
- Միելոիդ շարքի բջիջներ (երբեմն):
Թիրախ բջիջների ճանաչման և քիլլինգի մեխանիզմները տարբերվում են միելոիդ բջիջներին բնորոշ մեխանիզմներից: CTL-ը ճանաչում են հակածիններ, որոնք ներկայացված են MHC I-ով, իսկ NK-բջիջները արձագանքում են այն բջիջներին, ովքեր չեն էքսպրեսում մակերեսին MHC մոլեկուլներ:
CTL-ը և NK-ը ճանաչում են թիրախը տարբեր մեխանիզմներով'
- CTL-ը ճանաչում են սպեցիֆիկ հակածիններ (օր.' վարակված բջիջների վիրուսային պեպտիդները), որոնք ներկայացված են MHC մոլեկուլներով: CTL մեծ մասը CD8+ T-բջիջներ են, որոնք ճանաչում են հակածինները MHC I մոլեկուլների հետ համալիրում, բայց որոշ CD4+ բջիջներ նույնպես ունեն ցիտոտոքսիկ հատկություններ, սակայն ճանաչում են հակածինը MHC II կազմում:
- NK-բջիջները ճանաչում են թիրախ բջիջներ, որոնք չունեն մակերեսային MHC I' օգտագործելով դրա համար տարբեր ընկալիչներ: Դրական (ցիտոտոքսիկ) պատասխանի դեպքում NK-բջիջները ի վիճակի են փոխազդել Fc-ընկալիչներով (CD 16) հակամարմինների հետ, որոնք արդեն կապվել են թիրախ բջջի մակերեսի հակածնին. այս գործընթացը կոչվում է հակամարմին-կախյալ բջջային ցիտոտոքսիկություն (ADCC):
CTL-ի կարևորագույն գործառույթը վիրուսով ախտահարված բջիջների էլիմինացիան է: Գրեթե բոլոր կորիզավոր բջիջներում էքսպրեսվում են MHC I մոլեկուլներ և եթե բջիջը վարակվում է, ապա նրանք կարող են ներկայացնել վիրուսային հակածինները CD8+ ցիտոտոքսիկ լիմֆոցիտներին: Պրոտեասոմներում մասնակի քայքայված բջջի սպիտակուցները մտնում են էնդոպլազմատիկ ցանց, որտեղ կապակցվում են MHC I-ի հետ և գնում դեպի բջջի մակերես:
CTL և NK բջիջները կոմպլեմենտար են ազդում վիրուսով վարակված բջիջների դեմ իմունային պատասխանի ընթացքում:
Մի շարք վիրուսներ, հատկապես' հերպեսվիրուսները, կիրառում են մեխանիզմներ, որն օգնում է նրանց խույս տալ CTL կողմից ճանաչումից: Այդպիսի վիրուսների մոտ իջած է MHC մոլեկուլների էքսպրեսիան կամ նրանք արտադրում են սպիտակուցներ, որոնք հեռացնում են MHC մոլեկուլները էնդոպլազմատիկ ցանցից'իջեցնելով քայքայված վիրուսային պեպտիդների ներկայացման հավանականությունը բջջի մակերեսին: Քանի որ NK բջիջները ճանաչում են MHC I դասի մոլեկուլները կորցրած բջիջները, ապա կարելի է եզրակացնել, որ երկու բջիջների պաշտպանական ազդեցությունը ունի կոմպլեմենտար բնույթ:
- NK լիմֆոցիտները իրականացնում են <<անձնագրային>> հսկողություն, այսինքն' ստուգում են բջջի կողմից MHC I դասի մոլեկուլների առկայությունը:
- CTL-ն հսկում են սպեցիֆիկ իդենտիֆիկացիան, որը արտացոլվում է <<անձնագրում>> (այսինքն' հակածնային սպեցիֆիկությունը):
Մեկ CTL-ն ի վիճակի է սպանել շատ թիրախ բջիջներ: Դրա համար այն պետք ունենա հետևյալ հատկությունները'
- Կայունություն սեփական քիլլերային մեխանիզմների դեմ,
- Ի վիճակի լինեն անջատվել մահացած բջիջ թիրախներից:
Ցիտոկինով ակտիվացված բջիջ-քիլլերները NK դասին են պատկանում: 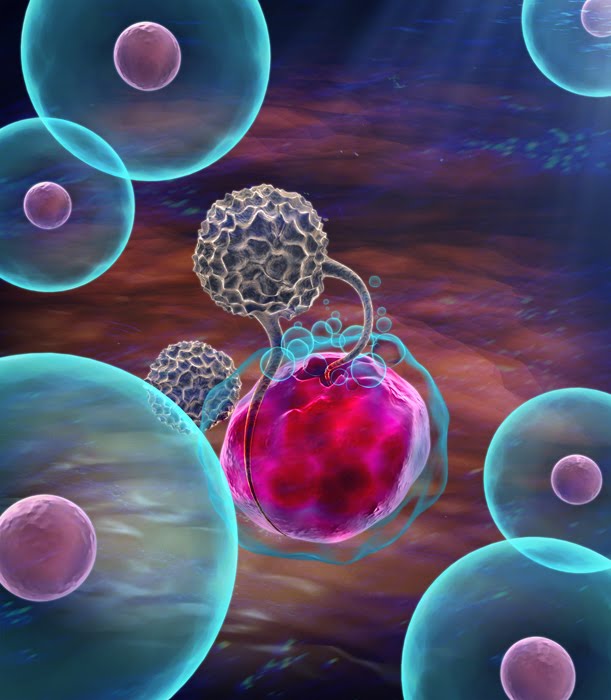
Ուռուցքների բուժման համար արդյունավետ միջոցներ հայտնաբերելու ուսումնասիրությունը վաղուց է գրավել իմունոլոգների ուշադրությունը: Մեթոդներից մեկը հիվանդի սեփական լիմֆոցիտների ակտիվացումն է in vitro' IL-2-ի օգնությամբ և հետագա հետ ներմուծումը օրգանիզմ: Այս բջիջները սկզբում ստացվել էին արյունից և փայծաղից և հայտնի են որպես ցիտոտոքսինով ակտիվացված քիլլերներ: Նրանց առաջին անվանումը' LAK-բջիջներ է (լիմֆոկիններով ակտիվացված քիլլերներ): Նրանք'
- Ունեն բարձր, MHC -ով չսահմանափակված (ռեստրիկցիա) ցիտոտոքսիկություն:
- Առաջանում են NK-ից չտարբերվող ցողունային բջիջներից: Հնարավոր է, նրանք առանձին պոպուլյացիա չեն, այլ առաջանում են ակտիվացման արդյունքում:
NK-բջիջները' էքսպրեսում են բազմազան ընկալիչներ
NK-բջիջների մեծ մասը առաջանում են մեծ գրանուլյար լիմֆոցիտներից (LGL), որոնք արյան լիմֆոցիտների 5%-ն են կազմում: NK մեծ մասը'
- Ունեն CD3-, CD16+, CD56+, CD94+ մարկերներ,
- Չունեն TCR-ի վերակազմավորման գեներ:
Գոյություն ունեն քիիլինգի հետ ասոցիացված ընկալիչներ'
- Առաջին խումբը II տիպի թաղանթային գլիկոպրոտեիններ են (նրանց C-ծայրային հատվածը գտնվում է բջջից դուրս), և պարունակում է C-տիպի լեկտինային դոմեն (Ca2+-կախյալ) /սրանք համարվում են KAR'քիլլինգ ակտիվացնող ընկալիչներ/:
- Երկրորդ խումբը Ig գերընտանիքին պատկանող քիլլինգ ընկճող ընկալիչներ են (KIR):
Վերջին տարիների ձեռքբերումն է հատուկ HLA-G մոլեկուլների հայտնաբերումը, որը էքսպրեսվում է միայն տրոֆոբլաստի կողմից, հանդիսանում է ինհիբիտոր, որը ընկերքին տալիս է կայունություն բոլոր տիպի NK-բջիջների հանդեպ: Ֆետալ բջիջները ընկերքի ձևավորումից հետո մտնում են մոր արյան հուն: Ներկայումս քննարկվում է, թե ինչպես է HLA-G-ն ճանաչվում NK-կողմից: Նրա լիգանդներից մեկն է ILT-2-ը: HLA-G-ի առաջատար պեպտիդը HLA-E-ով ներկայացվում է CD94-ին:
NK-բջիջները ընկալիչների օգնությամբ ճանաչում են իրենց թիրախին:
Թիրախին ճանաչելու համար NK-բջիջները օգտագործում են տարբեր ընկալիչներ, այդ թվում'CD2, Cd16 և CD69, ինչպես նաև' ցիտոտոքսիկությունը ընկճող ընկալիչներ: Fc-ընկալիչը կպչում է թիրախ բջջի մակերեսին գտնվող Ig-ին և միջնորդում է ADCC-ն: Առաջ այդ գործառույթը վերագրում էին K-բջջին, բայց այն կարող են կատարել այլ Fc-ընկալիչ ունեցող բջիջներ, այդ թվում և T-բջիջները: Fc կրող միելոիդ բջիջները նույնպես ունեն ADCC, բայց մեխանիզմը, հավանաբար, տարբերվում է: ADCC-ի հավանական թիրախներն են'
- Վիրուսային հակածինը բջջի մակերեսին,
- MHC մոլեկուլները,
- Ուռուցքների որոշ էպիտոպներ:
Ցիտոտոքսիկությունը պայմանավորված է ուղղակի միջբջջային փոխազդեցությամբ, ցիտոկիններով և պարունակվող հատիկների էկզոցիտոզով:
CTL և NK բջիջները քիլլինգ կատարում են տարբեր մեխանիզմներով, որոնցից են'
- Ուղղակի ազդեցություն (cell to cell)' մակերեսային մոլեկուլներով:
- Ցիտոկիններով միջնորդված ազդակի օգնությամբ:
Բացի դա,CTL և NK-ն ունեն հատիկներ, որոնք պարունակում են սպիտակուցներ: Վերջիններս արտազատվելիս ի վիճակի են քայքայել թիրախ բջիջները, մոտ գտնվելով բջջաթաղանթին: Այս մեխանիզմների զուգակցումը տարբեր ցիտոտոքսիկ բջիջների մոտ կարող է տարբերվել: Ցիտոտոքսիկ ազդակը կարող է հաղորդվել Fas կամ TNF -ընկալիչի օգնությամբ, որն առկա է թիրախ բջջի վրա:
Ցիտոտոքսիկ ազդակը կարող է հաղորդվել Fas կամ TNF -ընկալիչի օգնությամբ, որն առկա է թիրախ բջջի վրա:
CTL-ն ազդակը փոխանցում են ընկալիչներով, որոնք պատկանում են TNF ընկալիչների ընտանիքին:
- Fas (CD95),
- TNF-ընկալիչ:
CD4+ և CD8+ բջիջները առաջացնում են բջջի մահ'էքսպրեսելով Fas (FasL), որը TNF-ընտանիքի անդամ է: FasL-ն ճանաչում է մակերեսային Fas սպիտակուցը, որը էքսպրեսիայի է ենթարկվում շատ բջիջների կողմից: Խաչաձև կապման ընթացքում տրիմեր Fas և մահվան դոմեններ, որոնք գտնվում են Fas-ի ցիտոպլազմատիկ հատվածում, որոնք ասոցիացված են FADD մոլեկուլի հետ: FADD-ն իր հերթին կապվում է կասպազ-8-ի կամ 10-ի հետ'առաջացնելով Ca2+-կախյալ ապոպտոզ: Ակտիվացված կասպազ-8-ը քայքայում է և ակտիվացնում է այլ կասպազներ' ի լրումն սեփական ապոպտոզային ազդեցության:
TNF-ընկալիչի ընտանիքի մյուս անդամները, որոնք ունեն մահվան դոմեններ ցիտոպլազմատիկ հատվածում, օր.' TNFR-1-ը, լիգանդի հետ փոխազդելիս նույնպես ի վիճակի են խթանել կասպազ-կախյալ բջջային մահը համանման մեխանիզմով: Բջջի մահը խթանելու ունակությունը որոշվում է ցիտոպլազմատիկ հատվածում մահվան դոմենների առկայությամբ: TNF-ընկալիչների անդամները, որոնց մոտ մահվան դոմենը բացակայում է, այդպիսի ունակություն չունեն:
CTL-ի հատիկները պարունակում են գրանզիմներ և պերֆորին, որոնք կոչվում են լիտիկ հատիկներ: Թիրախ բջջի ճանաչման ժամանակ այդ հատիկները գնում են դեպի բջջային հպման հատվածը (հատված, որը կոչվում է իմունաբանական սինապս) և ձերբազատում ամբողջ պարունակությունը երկու բջիջների միջև եղած նեղ տարածության մեջ: Պերֆորին սպիտակուցը առաջացնում է անցքեր և գրանզիմ ֆերմենտները թափանցում են թիրախ բջիջ: Պերֆորինը մոնոմեր սպիտակուց է, որն առաջացնում է անցքեր: Չնայած NK CTL-ն օգտագործում են թիրախի ճանաչման տարբեր մեթոդներ, սակայն նրանց լիտիկ մեխանիզմները միանման են: Կարևոր դեր է խաղում պերֆորինը'մոնոմեր սպիտակուց, որն առաջացնում է անցքեր' կոմպլեմենտի C9 բաղադրիչին համանման: Հատիկների ներսում պերֆորինը ակտիվ չէ, սակայն ենթարկվում է կոնֆորմացիոն ակտիվացման կախված Ca2+ խտությունից: C9-ի նման պերֆորինը ձևավորում է հոմոպոլիմերներ, որոնք ներդրվում են թաղանթի մեջ' առաջացնելով 16 նմ տրամագծով կլոր անցքեր:
Ի տարբերություն C9-ի' պերֆորինը ունի դոմեն, որն անմիջապես կապվում է թաղանթի ֆոսֆոլիպիդներին Ca2+ առկայությամբ: Պերֆորինի պակասուրդի դեպքում բջիջը ունի ցածր ցիտոտոքսիկություն, սակայն ամբողջությամբ ցիտոտոքսիկ ակտիվությունը չի վերանում, ինչը խոսում է այլ մեխանիզմների առկայության մասին'հավանաբար, Fas և TNF-միջնորդված:
Գրանզիմները խթանում են ապոպտոզը'
Գրանզիմները սերինային պրոտեազներ են, որոնք թիրախ բջիջ են մտնում անցքերի միջոցով (անցքերը կազմված են պերֆորինով): Ցիտոպլազմայում գրանզիմները քայքայում են մի շարք նյութեր, որն արագ խթանում է ապոպտոզը:
- Գրանզիմ B-ն քայքայում է որոշ պրոկասպազներ' ակտիվացելով կասպազ-10, 3 և 7-ը, որը բերում է ապոպտոզի խթանման:
- Գրանզիմ A-ն կասպազ-անկախ մեխանիզմով իրականացնում է ապոպտոզի ակտիվացում: Այն ազդում է SET-ի (էնդոպլազմատիկ ցանցի հետ կապակցված սպիտակուցային համալիր) բաղադրիչներից մեկի վրա'ակտիվացնելով ԴՆԹ-ազան, որը քայքայում է ԴՆԹ-ն և կորիզը:
- Գրանզիմ C-ն բերում է կասպազ-անկախ ապոպտոզի'չնայած մանրամասները անհայտ են:
CTL և NK-բջիջները իրականացնում են թիրախ բջջի քիլլինգ, այդ ընթացքում մնալով անվնաս: Դա պայմանավորված է'
- Պերֆորինը և գրանզիմները արտադրվում են ոչ ակտիվ նախորդող ձևերի տեսքով և ակտիվացվում են' ոչ մեծ հատվածների քայքայման միջոցով:
- Ակտիվացումը տեղի է ունենում միայն պերֆորինի' հատիկների միջից ձերբազատումից հետո: Ենթադրվում է, որ հատիկներում նրանց ոչ ակտիվ վիճակը պահպանվում է pH-ի, Ca2+-ի որոշակի մակարդակով, պրոտեոգլիկանների մասնակցությամբ, որոնք կապում են պերֆորինը և գրանզիմները:
Համենայնդեպս, CTL-ն ի սկզբանե կայունություն ունեն պերֆորինի հանդեպ, քանի որ հատիկների պարունակությունը արտազատում է իմունաբանական սինապսի հատվածում: Վերջերս հայտնաբերված է, որ կատեպսին-B-ի թաղանթ-կախյալ ձևը նպաստում է լիզիսի հանդեպ CTL կայունության առաջացմանը: Հատիկները թաղանթի վրա տեղակայվելով'կատեպսին B-ն քայքայում է պերֆորինը այն մասից, որը դեպի սինապսն է ուղղված: Բացի այդ, լիզիսի հանդեպ կայունությունը բարձրացնում են մի շարք այլ մեխանիզմներ: Այսպես, CTL-ն էքսպրեսում են'
- cFLIP սպիտակուց, որը ընկճում է կասպազ-8-ի քայքայումը և ապոպտոզի մեխանիզմների միացումը:
- պրոտեազների ինհիբիտոր-8 սերպինը (IP-8) արգելակոիմ է գրանզիմ B-ի ազդեցությունը:
Մակրոֆագերը, նեյտրոֆիլները և էոզինոֆիլները ոչ լիմֆոիդ ցիտոտոքսիկ էֆեկտոր բջիջներ են
Մակրոֆագերը վնասում են թիրախ բջիջը' օգտագործելով ոչ սպեցիֆիկ տոքսիկ էֆեկտոր համակարգեր կամ ցիտոկիններ:
Որոշ ոչ լիմֆոիդ բջիջներ ևս կարող են լինել ցիտոտոքսիկ այլ բջիջների և միկրոօրգանիզմների նկատմամբ'ներառյալ բակտերիաներ և պարազիտներ: Ցիտոտոքսիկ ազդեցությունը կարող է լինել սպեցիֆիկ կամ միջնորդավորված մի շարք ոչ սպեցիֆիկ թունավոր նյութերով: Մասնավորապես, մակրոֆագերը և նեյտրոֆիլները էքսպրեսում են FcgRI և FcgRII ընկալիչներ, որոնք օժտում են այդ բջիջներին ուռուցքները ADCC մեխանիզմով քայքայելու հատկությամբ:
Սովորաբար ախտածին միկրոօրգանիզմները, որոնք մակրոֆագերի և նեյտրոֆիլների կողմից ֆագոցիտոզի են ենթարկվում, քայքայվում են ֆագոլիզոսոմի ներսում'ենթարկվելով թունավոր մոլեկուլների և ֆերմենտների ազդեցությանը որոնցից են'
- թթվածնի ակտիվ ձևերը, տոքսիկ օքսիդանտներ և ազոտի օքսիդ,
- արտազատվող մոլեկուլներ (նեյտրոֆիլների դեֆենզիններ, լիզոսոմալ ֆերմենտներ և ցիտոստատիկ սպիտակուցներ):
Եթե ֆագոցիտը ի վիճակի չէ ինտերնալիզացիայի ենթարկել թիրախ բջիջը, ապա միջնորդանյութերը դուրս են թափվում արտաբջջային միջավայր և բջիջների տեղային վնասում առաջացնում: Այդ ազդեցությունը կոչվում է անավարտ ֆագոցիտոզ և տեղի է ունենում, եթե բջիջը իր ընկալիչների շնորհիվ փոխազդում է թիրախի հետ, որը չափազանց մեծ է կուլ տալու համար: Միջնորդանյութերը, ազդելով թիրախի վրա, վնասում են նրանց, սակայն ապոպտոզի չեն ենթարկում, այլ առաջացնում են նեկրոզ և բորբոքում: Բացի դրանից, ակտիվացված մակրոֆագերը, արտադրելով TNF, առաջացնում են ապոպտոզ'NK և CTL բջիջներին համանման: Այսպիսով, մակրոֆագերն ի վիճակի են խթանել ապոպտոզը, առաջացնել նեկրոզ կամ երկուսն իրար հետ'կախված նրանց ակտիվության վիճակից և թիրախ բջջի հատկություններից:
Էոզինոֆիլների ցիտոտոքսիկությունը պայմանավորված է նրանց հատիկների էկզոցիտոզով 
Հասուն էոզինոֆիլները բնորոշվում են հատիկների պարունակությամբ, որոնք ունեն բյուրեղանման միջուկ և ներկվում են էոզինով: Էոզինոֆիլներն ունեն թույլ ֆագոցիտար հատկություններ. ակտիվանալով' նրանք կուլ են տալիս որոշ բակտերիաներ, սակայն նրանց կողմից բակտերիայի ներբջջային սպանումը նեյտրոֆիլների նմանատիպ ազդեցությունից ավելի թույլ է:
Էոզինոֆիլների հիմնական գործառույթը ակտիվացումից հետո հատիկների տոքսիկ բաղադրիչների արտազատումն է, ուստի նրանք միկրոօրգանիզմի արտաբջջային մահ են առաջացնում, հատկապես այնպիսի խոշոր պարազիտների, ինչպիսիք են շիստոսոմները:
Էոզինոֆիլների հատիկները պարունակում են'
- գլխավոր հիմնային սպիտակուց (MBp). սա բյուրեղային միջուկի պարունակությունն է: Այն վնասում, երբեմն էլ սպանում է պարազիտներին, սակայն ի վիճակի է նաև սեփական բջիջները վնասել:
- Էոզիլոֆիլների պերօքսիդազա (EPO. հետերոդիմեր հեմոպրոտեին է, որը ունի արտահայտված կատիոնային հատկություններ, որը օքսիդացնում է մի շարք սուբստրատներ, այդ թվում' հալիդների իոններ' առաջացնելով հիպոհալիդներ: Սա որոշ պարազիտների ամենաարդյունավետ քիլինգի մեխանիզմն է էոզինոֆիլների կողմից:
- Էոզինոֆիլների կատիոնային սպիտակուց (ECP). սպեցիֆիկ տոքսին է, որը պարազիտների քիլինգ է ապահովում, հատկապես շիստոսոմուլների: Այս մոլեկուլը ռիբոնուկլեազ է, որը իր բարձր լիցքի շնորհիվ կապվում է բացասական լիցքավորված մակերեսի հետ: Հավանաբար այն առաջացնում է թաղանթային անցքեր, որի միջոցով այլ միջնորդանյութեր թափանցում են թիրախի մեջ:
Էոզինոֆիլները արտադրում են նաև այլ մոլեկուլներ' լիպոֆոսֆոլիպազա և էոզինոֆիլների նեյրոտոքսին (EDN), որը նույնպես ռիբոնուկլեազ է, բայց արտահայտված նեյրոտոքսիկ հատկությամբ:
Զանազան գործոններ կարող են առաջացնել էոզինոֆիլների հատիկազերծում '
- IgG-ով պատված պարազիտների կապվելը մակերեսային FcγRII ընկալիչներին խթանում է որոշ միջնորդանյութերի արտադրում, այդ թվում' ECP-ի, բայց ոչ EPO-ի:
- FcεRII-I հետ փոխազդեցությունը բերում է EPO-ի, բայց ոչ ECP-ի արտադրության:
Պրազիտների մահը առաջանում է հպում-կախյալ հատիկազերծման կամ հյուսվածքներում տոքսինների տեղային ազդեցության հետևանքով: Մի շարք ցիտոկիններ ուղղակիորեն կարող են առաջացնել հատիկազերծում in vitro'
- IL-3
- IL-5
- GM-CSF
- TNF
- IFNβ
- PAF(platelete activating factor).
Այս միջնորդանյութերը նաև ուժեղացնում են ADCC-միջնորդված հատիկազերծումը:
Էոզինոֆիլները կարևոր դեր են խաղում բորբոքման ֆոնի վրա առաջացող ախտահարումների ժամանակ, հատկապես' աղիների, մաշկի, շնչուղիների ատոպիկ հիվանդությունների դեպքում, որոնք հաճախ ասոցիացվում են ֆիբրոզ պատասխանի հետ: Դրա օրինակ են հանդիսանում ատոպիկ էկզեման, ասթման և աղիների բորբոքային հիվանդությունը:
Էլեկտրոնային նյութի սկզբնաղբյուրը ՝ Doctors.am
Նյութի էլէկտրոնային տարբերակի իրավունքը պատկանում է Doctors.am կայքին










